Hari:Selasa, 1 oktober 2019
Nama:Andre Winata
Nim:C1061191103
Teori Asam Dan Basa
Definisi Bronsted-Lowry. Asam adalah Zat yang menyediakan Proton, dan Basa menerima proton.. Pengertian Asam Basa
Asam dan basa merupakan zat kimia yang banyak digunakan dalam kehidupan sehari hari.
1. Asam
Istilah asam (acid) berasal dari bahasa Latin “Acetum” yang berarti cuka, karena diketahui zat utama dalam cuka adalah asam asetat.secara umum asam yaitu zat yang berasa masam.
2. Basa
Basa (alkali) berasal dari ahasa arabyang berarti abu. Secara umum basa yaitu zat yang berasa pahit bersifat kaustik.
Mengidentifikasi asam – basa dengan kertas lakmus

Asam dalam pelajaran kimia adalah senyawa kimia yang bila dilarutkan dalam air akan menghasilkan larutan dengan pH lebih kecil dari 7. Dalam definisi modern, asam adalah suatu zat yang dapat memberi proton (ion H+) kepada zat lain (yang disebut basa), atau dapat menerima pasangan elektron bebas dari suatu basa. Atau Asam adalah zat (senyawa) yang menyebabkan rasa masam pada berbagai materi. Contoh asam : jeruk nipis, lemon, dan tomat. Ciri - ciri : - Rasanya asam
- Dapat menimbulkan korosif
- Mengubah kertas lakmus biru menjadi merah
- Ph < 7
- Menghasilkan ion H+
- Dapat menimbulkan korosif
- Mengubah kertas lakmus biru menjadi merah
- Ph < 7
- Menghasilkan ion H+
- Dapat menimbulkan korosif
- Mengubah kertas lakmus biru menjadi merah
- Ph < 7
- Menghasilkan ion H+
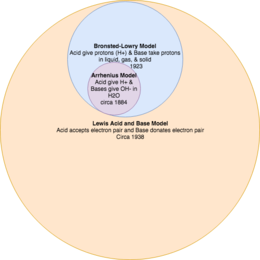
Definisi asam:
- Menurut Boyle: asam adalah zat yang dapat memerahkan lakmus biru
- Menurut Arrhenius: asam adalah zat yang jika dilarutkan dalam air akan melepaskan ion hidrogen (H+)
- Menurut Bronsted-Lowry: asam adalah pendonor proton (H+)
- Menurut Lewis: asam adalah akseptor elektron
Asam organik
Asam organik adalah asam karboksilat atau asam yang terbentuk karena persenyawaan dengan senyawa organik (misalnya hidrokarbon).
Contoh asam organik:
- Asam asetat (CH3COOH)
- Asam benzoat (C6H5COOH)
- Asam format (HCOOH)
Semua asam organik adalah asam lemah.
Asam anorganik
Asam anorganik adalah asam yang terbentuk karena persenyawaan dengan senyawa anorganik (misalnya hidrogen dengan klorin). Asam anorganik ada yang merupakan asam kuat, yaitu:
- Asam sulfat (H2SO4)
- Asam klorida (HCl)
- Asam nitrat (HNO3)
- Asam bromida (HBr)
- Asam iodida (HI)
- Asam klorat (HClO4)
Asam selain asam-asam di atas merupakan asam lemah, contoh:
- Asam askorbat
- Asam karbonat
- Asam sitrat
- Asam etanoat
- Asam laktat
- Asam fosfat
Basa menurut Svante Arrhenius

Garam atau nama senyawa kimianya "Natrium Klorida" (Nacl) dalam pelajaran kimia adalah senyawa ionik yang terdiri dari ion positif (kation) dan ion negatif (anion), sehingga membentuk senyawa netral (tidak bermuatan). Rumusnya : Asam + Basa ~ Garam + Air
Indikator terbagi menjadi dua yaitu : 1). Indikator Alami
adalah indikator yang terbuat dari
ekstrak tumbuh - tumbuhan tertentu
yang memiliki warna.
Contohnya ada :
1. Kunyit
Dalam asam berwarna kuning cerah
~ || ~ basa berwarna jingga
2. Kubis kol merah antosian
Dalam asam berwarna merah
~ || ~ basa berwarna hijau (basa lemah)
Kuning (basa kuat)
3. Ekstrak bunga kembang sepatu Dalam asam berwarna merah cabe ~ || ~ basa berwarna hijau2). Indikator Buatanadalah indikator yang dibuat di pabrik. Contohnya ada : 1. Asam Dalam lakmus merah berwarna merah ~ || ~ biru berwarna merah 2. Basa Dalam lakmus merah menjadi biru ~ || ~ biru menjadi biru 3. Netral
Makan makanan asam boleh, tapi jangan kebanyakan ya (Sumber: Giphy.com)
SIFAT ASAM DAN BASA
Asam dan basa merupakan dua senyawa kimia yang sangat penting dalam kehidupan sehari-hari kita. Secara umum, zat–zat yang memiliki rasa masam itu mengandung asam, misalnya asam sitrat pada jeruk, asam asetat pada cuka makanan, serta asam benzoat yang digunakan sebagai pengawet makanan.
Kemudian, basa adalah senyawa yang mempunyai sifat licin, rasanya pahit seperti obat dan sabun, kemudian ada beberapa jenis basa yang bersifat korosif (penyebab karat) dan kausatik (merusak kulit).
Meskipun asam dan basa dapat dibedakan dari rasanya, tetapi tidak disarankan lho ya (dilarang) untuk mencicipi asam atau basa yang ada di laboratorium, berbahaya, nanti kamu kenapa-kenapa lagi, soalnya kandungannya itu beda.
Reaksi asam–basa merupakan reaksi kimia yang melibatkan pereaksi asam dan basa, yang dapat digunakan dalam menentukan pH. Beberapa kerangka teoritis menyediakan konsepsi alternatif bagi mekanisme reaksi dan aplikasinya dalam penyelesaian masalah terkait; kerangka tersebut dikenal sebagai teori asam–basa, sebagai contoh, teori asam basa Brønsted–Lowry.
Pentingnya reaksi ini menjadi terlihat jelas dalam analisis reaksi asam–basa bagi spesi fasa gas dan cair, atau ketika sifat suatu asam dan basa tidak terlihat begitu jelas. Konsep pertama reaksi ini dikemukakan oleh kimiawan Perancis Antoine Lavoisier, sekitar tahun 1776.[1]
-1.gif?width=600&height=365&name=giphy%20(1)-1.gif)
Komentar
Posting Komentar